
我们提供专业的注册申请编辑和出版服务,帮助您应对复杂的化学药品、生物制品和医疗器械申报工作。我们确保递交材料格式正确,符合各国监管要求。我们帮您全程管理注册申请,从提交计划到正式提交。

我们提供全面的更新、修订和再注册服务,确保您的资料始终符合最新监管要求。通过积极应对监管变更,我们帮助您提前规划,确保顺利应对各种挑战,并保持产品在整个生命周期内的注册合规性。
康茂峰的资深注册专家拥有丰富的行业知识和经验,能够为您的全球申请制定有效的策略。我们提供量身定制的咨询服务,帮助您了解申请流程、识别潜在问题,并优化方法,以加快审批进度。

我们具备支持全球递交能力,助您扩展国际申请。我们的专业团队能处理不同国家的各种递交格式,包括eCTD等格式,以满足美国FDA、欧盟EMA、日本PMDA和中国NMPA等各个药监部门的要求,为您的全球注册提供全面支持。

我们采用严格的质量控制流程,确保您的递交材料准确无误,并符合所有监管标准。通过全面的质量控制,我们确保资料符合最新法规,从而最大限度地减少因不合规导致申请被拒的风险。
我们的专家能够协助客户优化申报资料管理流程,支持新兴市场客户顺利从纸质过渡到eCTD。我们还能协助您将建立全面的数据可视化解决方案,以提升注册运营管理的效率和透明度。
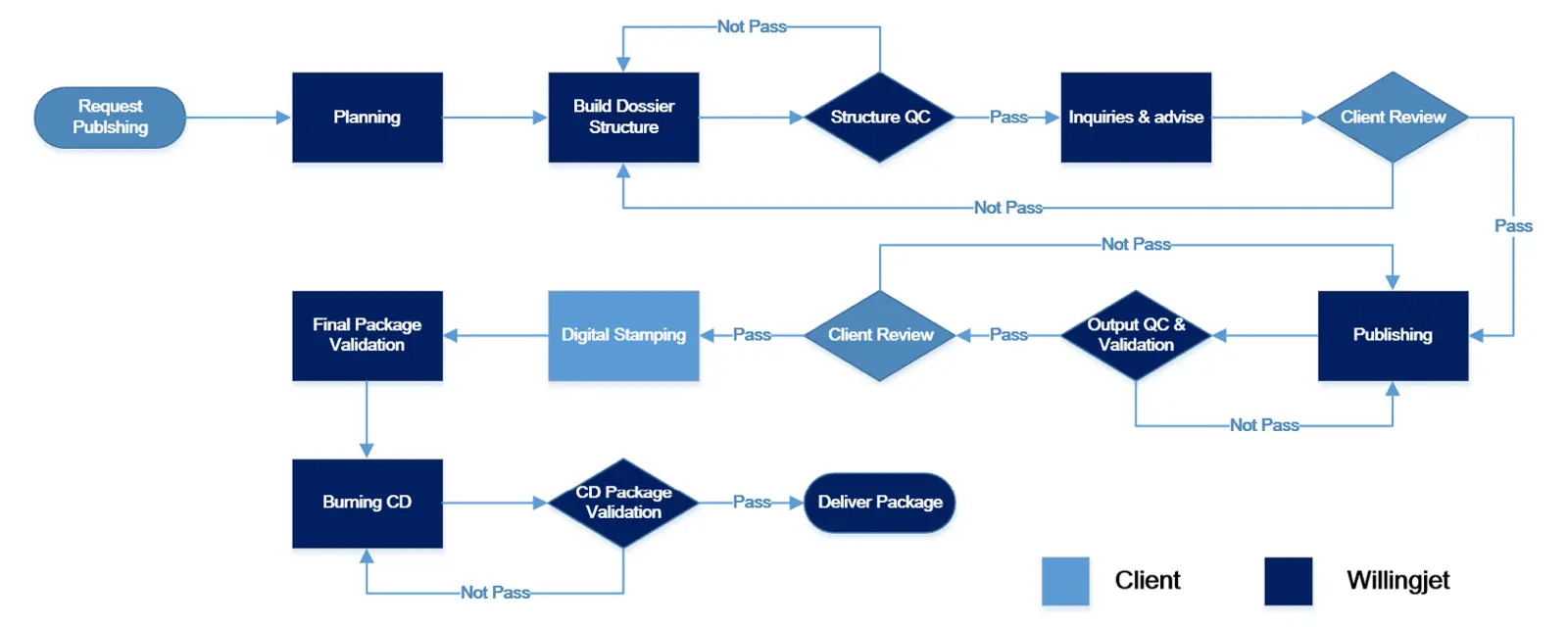
下图展示了康茂峰注册运营服务的标准流程。在实际项目中,我们能够根据客户的具体需求,选择使用客户现有的系统或我们自有的系统,设计定制化流程以满足全流程或者部分支持的服务。下图以eCTD电子递交项目为例。
客户是一家全球领先的生物科技公司,专注于肿瘤创新疗法。在准备和递交突破性癌症疗法的新药上市申请(NDA)时,他们寻求了我们的专业帮助。随着这项革命性疗法即将获批,客户认识到精确的注册运营递交资料对于加快监管审批流程至关重要。
客户面临的挑战在于如何将大量复杂的临床和非临床数据汇总并对所有资料进行收集和编辑,最终整理成结构化的递交资料包。同时,他们还需要确保这些资料符合包括FDA(美国)和EMA(欧洲)在内的多个地区的严格监管要求。
决定与康茂峰合作后,我们为客户提供了一整套量身定制的全球注册运营服务。我们的注册运营专家团队与客户紧密合作,利用在抗肿瘤药物研发和注册事务方面的丰富经验,为他们制定了详细而周密的递交计划。
1.全面的文件管理:我们的团队仔细整理并汇总了所有必需的文件,包括临床试验数据、非临床研究结果和CMC信息,创建了结构化的注册申请资料包。
2.制定注册战略:我们与客户紧密合作,开发了一套高效的全球注册战略。这一战略不仅帮助识别和应对潜在的挑战,还优化了递交时间表,以确保在整个注册过程中实现最高效率和最佳效果。
3.全球递交管理:凭借丰富的全球注册申报经验,我们为客户精心准备并管理全球的注册申报资料,尤其是针对主要监管机构(如FDA和EMA),确保所有文件符合各地区的监管要求。
4.质量保证与修正:我们在每个递交阶段执行严格的质量检查,从而及时发现和纠正任何错误或不一致。我们全面支持管理监管机构提出的问询并协助客户完成相关答复,确保审批流程顺利进行。
加速审批进程:借助我们优化的注册运营服务,客户成功简化了注册资料准备流程,加快申报资料准备以及提交速度。我们不仅为客户选择了最佳流程,还在竞争激烈的市场环境中加速了审批过程,确保疗法能够按时上市。
合规保证:我们的全面注册合规策略确保所有提交的材料严格符合相关监管标准和要求。通过这种方法,我们大大降低了被拒绝或审批延迟的风险,帮助客户顺利推进其注册申请。
战略合作:与康茂峰建立战略合作伙伴关系后,客户不仅获得了专家的专业指导,还享受了量身定制的个性化支持和服务。这种合作使客户能够充分利用我们在成功递交方面的丰富经验,从而提升了申请过程的效率和效果。
与康茂峰合作后,该制药公司显著加快了肿瘤创新疗法的全球注册提交审批过程。我们提供的量身定制服务和战略专业知识不仅简化了递交流程,还确保了合规性,最终加速将挽救生命的治疗方式提供给急需的患者。
 什么是注册运营?
什么是注册运营?
注册运营的核心职责是根据要求的格式(如eCTD、NeES、电子版和纸质版)向药品监管部门提交注册资料。注册运营团队需与各部门紧密合作,确保所有提交的资料符合规定的格式和要求。
 什么是eCTD?
什么是eCTD?
电子通用技术文档(eCTD)是向药监部门递交注册申请的标准电子格式。全球制药和生物技术行业广泛采用eCTD,以其结构化和高效的方式满足监管机构的文件递交要求。
 为什么要求进行eCTD递交?
为什么要求进行eCTD递交?
电子递交的要求旨在保证监管审批过程的连贯性、条理性和高效性。许多监管机构,包括FDA、EMA和PMDA,都要求以这种格式提交材料,以简化流程并加速决策。
 eCTD在全球的实施情况如何?
eCTD在全球的实施情况如何?
大多数成熟市场强制要求使用电子递交格式,例如美国、欧盟、英国、澳大利亚和加拿大。其他市场,如海湾国家、瑞士、南非、中国和泰国,则自愿采用电子递交,以提高效率。
 你们的服务如何确保递交的资料符合监管标准?
你们的服务如何确保递交的资料符合监管标准?
我们根据最新的监管指南和要求不断更新服务,以确保合规性。我们通过全面的审查清单和质量保证流程,对您的递交资料进行逐项检查,确保所有文件符合监管机构所要求的标准和格式。
 贵司如何帮助我们制定全球递交策略?
贵司如何帮助我们制定全球递交策略?
我们可以帮助您制定全球递交策略。我们的专家精通各地区的注册运营流程,提供全方位的全球递交支持。此外,我们擅长同时管理多份申报资料,确保您在各个国家和地区的提交都能按时完成。
 在递交过程中出现错误怎么办?
在递交过程中出现错误怎么办?
如果在质量检查或递交给监管机构后的验证中发现任何错误,我们会及时处理和纠正这些问题。我们提供全面支持,帮助解决监管机构提出的问题,并进行必要的修订,确保审批流程的顺利推进。
 如何处理现有电子递交资料的更新或修改?
如何处理现有电子递交资料的更新或修改?
我们为您的电子递交资料提供全方位的全生命周期管理,包括更新、修订和再注册。我们的服务可确保您的资料得到及时更新,并符合最新的监管要求。
 贵司的电子递交服务有何优势?
贵司的电子递交服务有何优势?
我们的电子递交服务以其专业性、精准度和对客户成功的承诺在业内脱颖而出。我们提供个性化的关注和量身定制的策略,并利用广泛的监管知识,确保不仅满足合规要求,还帮助您的递交资料在竞争中占据优势。
 eCTD递交由哪些部分组成?
eCTD递交由哪些部分组成?
eCTD(电子通用技术文档)申请需要符合CTD(通用技术文档)的结构。CTD结构主要分为五个主要模块,模块1为区域性要求,模块2、3、4和5则为统一要求。。
模块1:行政综述信息:每个地区特定的行政管理信息。包括所有与递交资料相关的重要细节,如申请表、说明函和综合目录等。
模块2:药物的总体总结,包括质量、临床和非临床数据综述等。
模块3:质量相关的研究信息,详细描述药物的化学、制造和控制(CMC)信息。
模块4:非临床试验报告,包含药物在动物或其他非临床研究中的数据。
模块5:临床研究报告,涵盖所有临床试验阶段的详细信息和结果。
我们的注册运营服务简化了递交流程,减少了复杂性,并缓解了技术要求的压力。通过优化文件管理和递交时限,我们帮助您集中精力于创新,减轻了行政管理的负担。
我们拥有经验丰富的专家团队,能提前识别监管变更,确保您的递交资料符合最新法规和指导原则。通过这种前瞻性的策略,我们帮助您降低申请被拒的风险,并加快审批速度。
利用我们在全球递交资料方面的专业知识,您可以拓展产品的市场覆盖范围。无论是北美、欧洲还是亚洲,我们熟悉各地区的具体要求,能够助您顺利进入多样化的市场,实现真正的全球战略布局。
我们的优化注册运营服务能够显著缩短产品上市时间。通过高效的文件准备和递交策略,我们加快了审批过程,帮助您更快地将产品推向市场。
我们的注册事务专家团队将为您提供全面的专业支持,让您放心无忧。在整个申请过程中,我们将提供个性化的协助,确保专家的指导贯穿始终。
我们致力于维护数据安全和完整性,严格遵循最高标准。在整个递交过程中,我们采用先进的安全协议来保护您的敏感信息,确保数据的保密性和安全性。

 04 09 2024
04 09 2024

 12 05 2024
12 05 2024
 11 07 2024
11 07 2024

 02 07 2024
02 07 2024